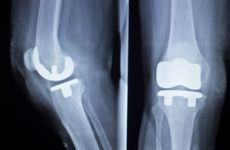
来自英国的临床研究人员正在开发一种诊断与假体关节植入物相关感染的方法,该方法有望在几小时内提供结果,而不是一周或更长时间。
这项工作利用了牛津纳米孔测序技术,本周早些时候在阿姆斯特丹举行的欧洲临床微生物学和传染病大会上进行了展示,这是讨论该技术在患者周围快速诊断传染病的潜力的几场演讲之一。vwin德赢ac米兰合作
特蕾莎·斯特里特(Teresa Street)是纳菲尔德医学系的研究科学家,也是牛津大学人类科学研究所的遗传学讲师,她讨论了她的团队试图验证这项技术,作为诊断假体关节植入感染的完全无培养方法的一部分。vwin德赢ac米兰合作
为了说明当前的问题,斯特里特引用了英国国家联合登记处2017年收集的关节置换手术数据。在那一年进行的约11.3万例全膝关节置换手术中,有6500例(约6%)是翻修手术,其中近四分之一的手术是因为感染或怀疑感染而进行的。肘关节置换手术与感染相关的翻修手术的比例相似,而肩部和髋关节置换分别约为17%和16%。
斯特里特说,目前的金标准是从手术中收集的假体周围组织样本中进行细菌培养,尽管另一种选择是在盐水中从超声移植假体中进行细菌培养。
然而,她指出,组织样本的培养相对不敏感,检出率约为65%,而且是“一个非常繁忙的过程,有许多步骤”。她的团队想知道它是否可以通过在培养阴性病例中更快地检测,并直接从临床样本中检测,来提高对骨科设备感染的检测。
理论上,宏基因组测序可以完成所有这些事情。它主要涉及直接从临床样本中提取所有DNA或RNA,对其进行测序,并将其与参考基因组进行比较,以识别病原体。
Street和同事在一项研究中证明了使用Illumina MiSeq测序方法的原理发表于2017年临床微生物学杂志.他们设计的工作流程包括在手术过程中取出假体设备,然后将其置于生理盐水中,并对其进行超声处理,以获得大约40毫升的超声液——这基本上是“我们在实验室中可以轻松处理的最大体积,这使我们能够最大限度地从细胞中提取DNA,”斯特里特在ECCMID上说。
声波处理步骤可能会增加样品中可用的细菌细胞的数量,因为它破坏了细菌生物膜。从超声样本中提取DNA,清洗,并准备到文库中,然后对其进行测序。
斯特里特说,尽管他们获得了相对较高的物种水平的敏感性和特异性(两者都为88%),但他们为未来的研究学到了一些东西。
“我们了解到人类DNA确实存在问题,”她在ECCMID上说。“在我们97%的样本中,我们生成的90%以上的序列数据都是人类的,所以我们显然是把它扔掉了。”
他们还了解到,生成培养阴性样本的宏基因组图谱进行比较很重要,因为污染是一个问题。这种污染可能来自多种来源,包括样品收集、实验室中的样品处理,以及样品处理中使用的实际试剂盒和试剂。
最重要的是,他们了解到他们需要更多的测序读数,以便能够做更多的事情,而不仅仅是识别物种,这就是为什么该小组已经转向纳米孔测序。从本质上讲,纳米孔测序产生的更长的读取长度和额外的数据可以提高参考基因组的读取覆盖率。
“这很令人兴奋,”斯特里特说。“这是便携。您可以生成更长的读取长度,但关键是您可以实时分析数据。……在手术期间,你可以在隔壁的手术中使用它,这并不是一种延伸。”
在后续的电子邮件中,斯特里特指出,她的团队不得不对纳米孔测序方案进行了一些修改,最重要的是增加了一个更有效的人类DNA耗尽步骤。她说:“纳米孔文库准备使我们能够结合PCR扩增步骤,这使我们能够将更长的片段进行测序,并有更多的DNA进行实际测序。”
该小组还采用了牛津大学尼克·桑德森(Nick Sanderson)开发的生物信息学管道,称为CRuMPIT(临床实时宏基因组学病原体鉴定测试)。这个管道的关键组成部分包括一个名为离心机的程序,它正在进行分类分类,以及Minimap2,它正在将reads映射到参考基因组。CRuMPIT管道是描述于BMC基因组学纸去年出版。
在一项未发表的原理证明研究中,斯特里特的团队分析了之前Illumina研究遗留下来的DNA样本,迄今为止发现了极好的一致性。在少数情况下,他们还能够从以前的属级识别中识别出两个独立的物种(例如。蜡样芽胞杆菌而且b基因而不是芽孢杆菌。).
Street还指出,使用纳米孔测序技术,生成物种鉴定所需的读数的时间已经大大减少。
该小组目前正在考虑如何进一步优化他们的纳米孔测序方法。具体来说,他们正在测试一种基于洗涤剂的样品制剂,它可以选择性地溶解人类细胞,然后是一种内切酶,在进入细菌溶解步骤之前降解人类DNA。
他们还在测试牛津纳米孔的快速PCR条形码试剂盒,该试剂盒允许输入10纳克的DNA,以抵消在人类DNA消耗步骤中消耗大部分可存活DNA的事实。该试剂盒还采用了6分钟的PCR延伸步骤,从而产生更长的用于分析的片段,以及更多的PCR循环以提高产量。此外,它支持多路复用,从而降低了排序的总体成本。
到目前为止,Street说,他们使用这种改进方案的分析与培养测试有高度的一致性,事实上,他们已经能够检测出某些培养阴性的阳性物种。此外,在少数葡萄球菌到目前为止,他们已经能够鉴定出抗微生物药物耐药性基因。
在一个样本中,他们能够检测到两种不同的葡萄球菌他们可以识别其中一种生物(美国haemolyticus),其中一个他们不能。他们后来用MALDI-ToF质谱鉴定这种生物为美国caprae他们意识到他们最初无法检测到它,因为它不在他们的参考数据库中,这强调了一个事实,即宏基因组测序只能与所使用的参考数据库一样好。
史崔特的团队并不是第一个使用宏基因组测序来识别关节置换中的感染性生物的团队。由梅奥诊所的罗宾·帕特尔领导的团队开发了自己的鸟枪宏基因组学方法使用Illumina测序,也获得了有希望的结果,并认识到一些与斯特里特指出的相同的挑战——即减少样本中人类DNA的数量和最大化细菌DNA读取的困难。
Patel的团队还指出,数据分析是耗时的,需要专业的生物信息学专业知识,这两者都是常规实施的障碍。今年早些时候,帕特尔和同事们发表了一篇论文临床微生物学杂志评估了来自马里兰州罗克维尔CosmosID公司的生物信息学包,指出它有潜力提供“快速、可靠的细菌检测和识别,从超声液中提取宏基因组鸟枪测序数据,用于诊断假体关节感染。”斯特里特指出,尽管她和其他人的研究在早期取得了有希望的结果,“在考虑实施这种方法之前,还有很多工作要做。我们还没有在牛津纳米孔上用我们的新方法对足够多的样品进行测序,还不能以更统计的方式处理关于识别背景[和]污染读数的数据。在我们开始计算读取数字的界限或阈值之前,我们需要更多的数据,这样我们才能更有信心,我们所识别的代表了真正的感染。”
